Cómo convertir la reforma regulatoria de la UE en una plataforma de liderazgo industrial y clínico desde las filiales españolas.
Por Ehab Soltan
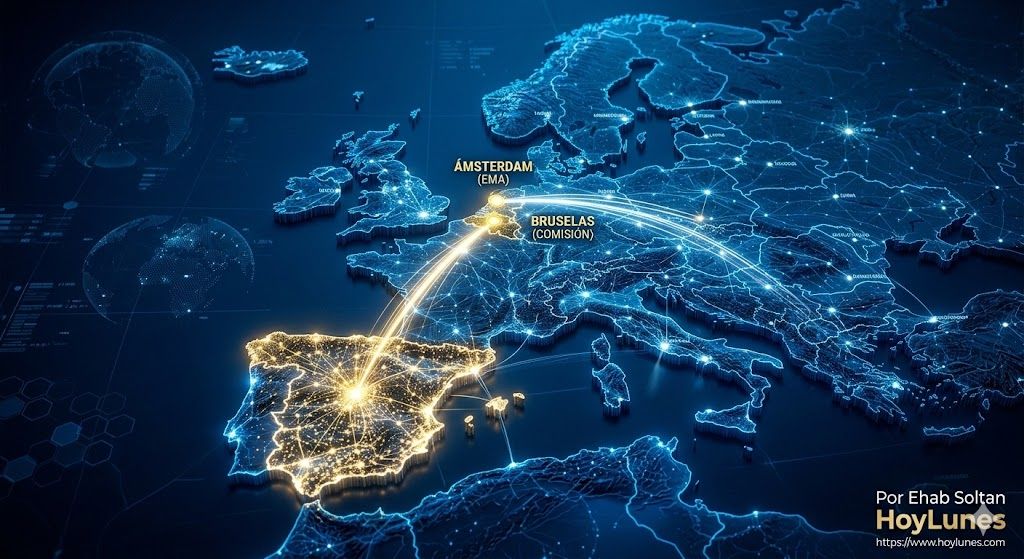
HoyLunes – Europa está redefiniendo las reglas del juego farmacéutico. La combinación de la reforma legislativa comunitaria, la aplicación progresiva del Reglamento de Evaluación de Tecnologías Sanitarias (HTA) y la consolidación del papel científico de la Agencia Europea de Medicamentos (EMA) está configurando un nuevo entorno competitivo. En este contexto, la pregunta estratégica para las multinacionales con sede en España no es defensiva —cómo adaptarse—, sino expansiva: cómo convertir a España en una plataforma de liderazgo dentro de la nueva economía regulatoria europea.
La Unión Europea avanza hacia un modelo que combina mayor exigencia científica con coordinación supranacional. El paquete de reforma farmacéutica impulsado por la Comisión Europea introduce ajustes en periodos de exclusividad e incentivos vinculados al acceso equitativo. Lejos de ser una amenaza, este rediseño puede consolidar un marco de previsibilidad para las compañías que sepan anticiparse.
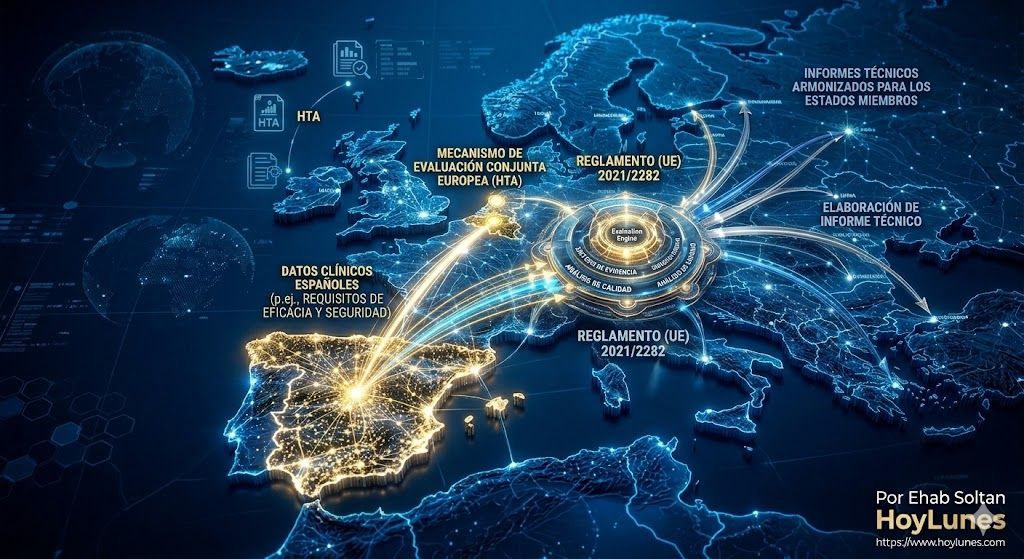
El Reglamento (UE) 2021/2282 introduce evaluaciones clínicas conjuntas obligatorias para determinados medicamentos innovadores. Esto implica que la evidencia comparativa y los datos de valor añadido ya no podrán diseñarse exclusivamente con lógica nacional. Para las filiales españolas, significa integrar antes la estrategia de generación de evidencia en la planificación global de lanzamientos, anticipando exigencias que afectarán simultáneamente a múltiples mercados europeos. La capacidad de coordinar ensayos, evidencia en vida real y posicionamiento terapéutico desde España puede convertirse en un activo estratégico ante las sedes centrales.
Para las filiales españolas, esta convergencia significa integrar la estrategia regulatoria local en la planificación global de sus matrices, aprovechando que España es hoy uno de los principales motores de exportación de productos de alta tecnología de la UE.
España como nodo competitivo en I+D clínica
España no es un actor periférico. Según la AEMPS, el país se sitúa consistentemente entre los líderes europeos en ensayos clínicos, destacando en oncología y enfermedades raras. Esta posición responde a factores estructurales críticos:
Red hospitalaria pública altamente cualificada y receptiva.
Investigadores de élite con elevada productividad científica.
Agilidad administrativa: España es uno de los países más rápidos de la UE en la puesta en marcha de ensayos gracias al Real Decreto 1090/2015.
Eficiencia operativa: Costes competitivos frente a otros grandes mercados europeos.
En la actual competencia global —con EE. UU. acelerando aprobaciones y Asia expandiendo su capacidad—, España ofrece un equilibrio único entre rigor científico y velocidad de ejecución.
La sostenibilidad como ventaja competitiva
El gasto farmacéutico representa entre el 15% y el 20% del gasto sanitario en la UE. Esta presión presupuestaria es una realidad, pero también una oportunidad para generar certidumbre. El modelo europeo, más cauteloso que el estadounidense, atrae a compañías que priorizan la reputación científica y el acceso ordenado.
El desafío será liderar modelos de precio y reembolso basados en valor y acuerdos de riesgo compartido. Aquellas filiales en España capaces de pilotar estos esquemas innovadores estarán mejor posicionadas para atraer inversiones de sus sedes globales.
Riesgos que requieren liderazgo corporativo
El entorno presenta incertidumbres que no deben ignorarse:
Ajustes en los periodos de exclusividad de datos.
Fragmentación autonómica en las decisiones de acceso al mercado.
Creciente exigencia de evidencia en vida real (RWE) post-autorización.
Enfrentar estos retos con liderazgo convierte la dificultad en ventaja competitiva. Las compañías con liderazgo en vacunas de nueva generación, inmunoterapia avanzada o terapias CAR-T tienen en España un laboratorio regulatorio ideal para consolidar su referencia interna.

Más allá del mercado: posicionamiento industrial
La «autonomía estratégica abierta» de la UE exige reforzar la producción local. El sector farmacéutico en España ya es un pilar industrial, situándose como el primer sector en I+D industrial del país. Las multinacionales tienen aquí la oportunidad de consolidar hubs logísticos y centros de excelencia que den servicio a toda la arquitectura europea.
Según datos sectoriales consolidados, la industria farmacéutica representa el primer sector industrial en inversión en I+D en España y uno de los principales exportadores de bienes de alta tecnología del país. Esta masa crítica no solo aporta empleo cualificado y capacidad productiva, sino también legitimidad para aspirar a mayores responsabilidades estratégicas dentro de los grupos multinacionales.
La movilización de fondos europeos a través de iniciativas como el PERTE para la Salud de Vanguardia refuerza este posicionamiento, al facilitar inversiones en terapias avanzadas, digitalización sanitaria y capacidades productivas críticas. Para las multinacionales, este entorno reduce el riesgo inicial de expansión y mejora la ecuación de retorno a medio plazo.
El debate no es ideológico; es estructural. ¿Será Europa un mero consumidor de innovaciones externas o un ecosistema propio competitivo? La respuesta reside en las decisiones corporativas que se tomen hoy desde Madrid o Barcelona.
Una invitación estratégica
HoyLunes aspira a ser la plataforma de reflexión para quienes entienden que la innovación no es un eslogan, sino una responsabilidad compartida. Las multinacionales con presencia en España tienen el incentivo de liderar la conversación sobre cómo integrar excelencia científica, competitividad industrial y acceso equitativo.
En un momento en que los comités globales de inversión evalúan dónde concentrar capital, talento y capacidades regulatorias, la posición de España no debe darse por supuesta. Las filiales que asuman un papel proactivo en la generación de evidencia, la negociación de modelos innovadores de acceso y la consolidación industrial estarán mejor situadas para influir en las decisiones estratégicas de sus matrices.
Europa ha trazado el marco. España dispone de las condiciones. La ventana de oportunidad está abierta. La diferencia entre consolidar liderazgo o perder centralidad dependerá de las decisiones estratégicas que se adopten hoy en las filiales españolas y se defiendan mañana en los comités globales.
Fuentes principales:
Comisión Europea – Pharmaceutical Strategy for Europe.
Agencia Europea de Medicamentos (EMA).
Reglamento (UE) 2021/2282 (HTA).
Agencia Española de Medicamentos y Productos Sanitarios (AEMPS).
OECD Health at a Glance.
`#Farmaindustria` `#EMA` `#InvestigaciónClínica` `#HoyLunes` `#EhabSoltan` `#SaludPública`
Este contenido es meramente informativo y no sustituye la consulta médica profesional.