De las vacunas combinadas de ARNm a terapias dirigidas para tumores pediátricos: la EMA impulsa un nuevo equilibrio entre innovación, beneficio clínico y responsabilidad social.
Por Ehab Soltan
HoyLunes – Desde los pasillos de su sede en Ámsterdam, la Agencia Europea de Medicamentos (EMA) no solo valida moléculas; está redefiniendo el marco operativo de la sanidad europea para la próxima década. A comienzos de 2026, Europa se sitúa en un punto de inflexión en el que la eficiencia tecnológica —representada por el ARNm— y la medicina de precisión —encarnada en la oncología pediátrica— obligan a replantear cuánto está dispuesta a invertir, y bajo qué condiciones, para sostener el progreso biomédico.
La era de la inmunización combinada: eficiencia en una sola dosis
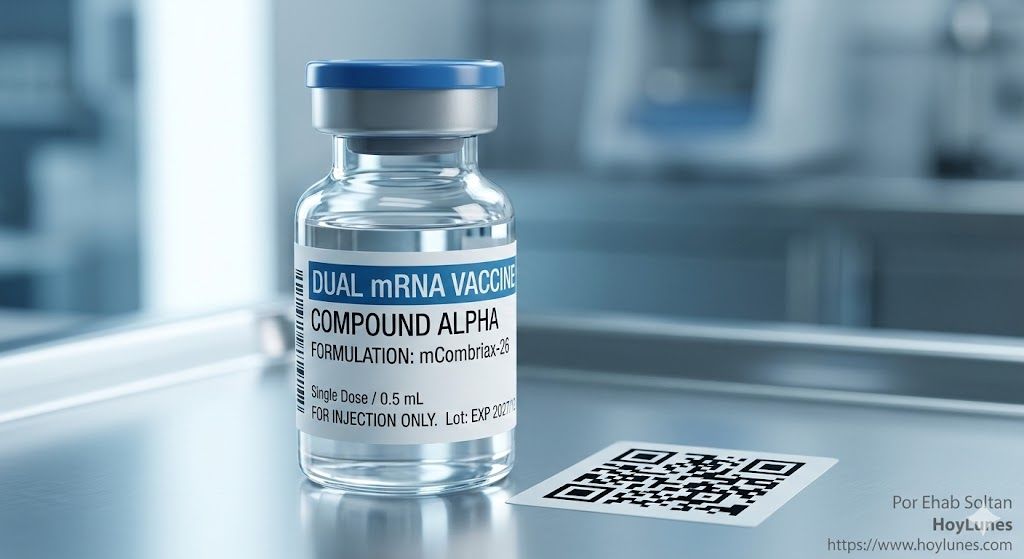
En febrero de 2026, el Comité de Medicamentos de Uso Humano (CHMP) emitió una recomendación positiva para mCombriax, la primera vacuna combinada de ARNm contra la gripe estacional y el SARS-CoV-2 destinada a mayores de 50 años. No se trata de una autorización rutinaria; marca el inicio de la normalización de la plataforma ARNm fuera del contexto de emergencia pandémica.
Al integrar dos protecciones en un único vial, la EMA envía una señal estratégica: la conveniencia clínica y la eficiencia operativa son ahora variables centrales de salud pública.
El engranaje institucional europeo
Conviene precisar que la EMA no “aprueba” medicamentos en sentido jurídico estricto. El CHMP emite una opinión científica basada en calidad, seguridad y eficacia; la decisión formal corresponde a la Comisión Europea, que concede una autorización válida en todos los Estados miembros. Posteriormente, cada país negocia precio y condiciones de reembolso.
Esta arquitectura separa deliberadamente evaluación científica y decisión económica, protegiendo tanto el rigor regulatorio como la sostenibilidad presupuestaria.
Proyecciones regulatorias e impacto presupuestario
Desde una perspectiva técnica, mCombriax anticipa la expansión de las vacunas polivalentes adaptativas. Es previsible que, en los próximos años, se consolide un marco de actualizaciones ágiles de cepas, combinando el modelo clásico de la gripe con la velocidad tecnológica del ARNm.
Impacto presupuestario potencial
Reducción de costes logísticos: La administración dual podría disminuir entre un 15 % y un 20 % los gastos operativos de las campañas al reducir visitas clínicas y exigencias duplicadas de cadena de frío.
Sostenibilidad macroeconómica: Aunque el precio unitario es superior al de vacunas proteicas tradicionales, la reducción de hospitalizaciones por coinfección puede compensar la inversión en un solo ciclo estacional.
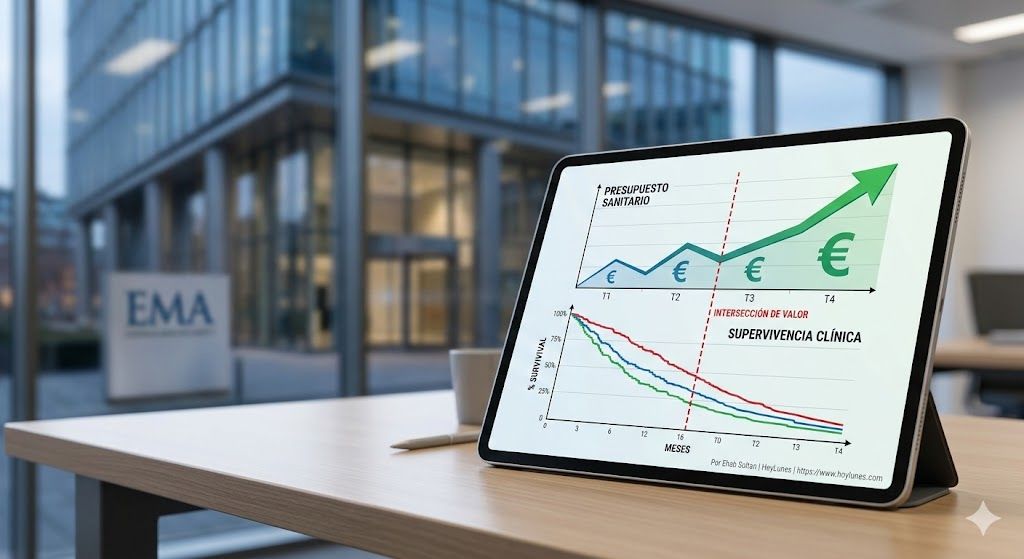
El gasto farmacéutico representa aproximadamente entre el 15 % y el 20 % del gasto sanitario total en la Unión Europea, con un crecimiento sostenido impulsado por terapias oncológicas y medicamentos huérfanos. En oncología, el incremento acumulado desde 2020 supera el 30 % en varios Estados miembros. La incorporación simultánea de vacunas combinadas y terapias de precisión obliga a revisar modelos de financiación en sistemas sometidos a envejecimiento demográfico y presión estructural.
Si las vacunas combinadas simbolizan eficiencia poblacional, la oncología pediátrica representa el otro extremo del espectro regulatorio: terapias altamente específicas dirigidas a cohortes reducidas pero clínicamente urgentes. Allí donde la inmunización optimiza sistemas, la medicina de precisión redefine el valor individual de cada vida.
Ojemda: cuando la precisión alcanza a los más vulnerables
El segundo eje de esta transformación es Ojemda (tovorafenib), indicado para determinados casos de glioma pediátrico de bajo grado (pLGG). Para los pacientes refractarios a cirugía o quimioterapia, las alternativas históricas han sido limitadas.
Con tasas de respuesta cercanas al 71 %, tovorafenib no solo frena el crecimiento tumoral; reduce la exposición a toxicidades sistémicas asociadas a esquemas tradicionales basados en carboplatino y vincristina, que implican neurotoxicidad acumulativa, mielosupresión y hospitalizaciones prolongadas.
Además, la supervivencia libre de progresión en pacientes refractarios ha sido históricamente reducida, con impacto cognitivo y endocrino significativo. En este contexto, un inhibidor selectivo
con perfil molecular dirigido no constituye únicamente un avance terapéutico; representa un cambio estructural en la evaluación riesgo-beneficio.
Sin embargo, su autorización reabre el debate sobre la medicina de nicho y la sostenibilidad de los fármacos huérfanos de alto coste.
Evidencia en el mundo real y modelos de pago
La EMA está reforzando mecanismos de Evidencia en el Mundo Real (RWE) para monitorizar estos tratamientos tras su comercialización. El desafío para los sistemas nacionales —como el SNS en España, el AIFA en Italia o el HAS/ANSM en Francia— será consolidar modelos de pago por resultados: financiación condicionada a beneficio clínico sostenido.
Este enfoque desplaza el riesgo financiero parcialmente hacia la industria y exige infraestructuras de datos robustas y transparentes.
Acceso, biosimilares y equilibrio presupuestario
En su reunión más reciente, el CHMP recomendó doce nuevos medicamentos y amplió seis indicaciones adicionales. Paralelamente, se intensificó el impulso a los biosimilares y medicamentos biológicos de segunda generación, instrumentos clave para contener costes y ampliar acceso.
La innovación pierde legitimidad si amplía brechas de desigualdad entre Estados miembros. En 2026, el papel regulatorio de la EMA se mide tanto por la calidad científica de sus dictámenes como por su impacto distributivo.
Europa frente a la FDA y la competencia global
Mientras la FDA estadounidense ha expandido mecanismos de aprobación acelerada, la EMA mantiene una orientación comparativa más prudente, centrada en el valor terapéutico añadido.
La diferencia es también cultural. El modelo estadounidense prioriza dinamismo de mercado; el europeo enfatiza solidez comparativa y evaluación incremental del beneficio clínico. Esta divergencia influirá en la competitividad biofarmacéutica de la próxima década, especialmente ante el crecimiento de la inversión china en biotecnología y ensayos descentralizados.
Europa enfrenta un dilema estratégico: evitar convertirse únicamente en evaluador regulatorio de innovaciones externas y consolidarse como motor propio de investigación traslacional.
Proyecciones 2026-2030
Descentralización de ensayos clínicos: mayor integración de telemedicina y dispositivos digitales para ampliar la participación geográfica.
Inteligencia artificial en farmacovigilancia: sistemas de detección temprana de eventos adversos capaces de reducir tiempos de reacción de meses a días.
No obstante, la aceleración regulatoria exige cautela. La dependencia creciente de datos intermedios, estudios de un solo brazo y RWE requiere revisiones periódicas estrictas y capacidad real de retirada si el beneficio no se confirma. La confianza pública depende de que la velocidad no sustituya al rigor.
El nuevo contrato social sanitario
En términos estructurales, la EMA actúa como mediadora de un renovado contrato social sanitario. La ciudadanía acepta financiar innovación de alto coste bajo la premisa de acceso equitativo y evidencia sólida. La industria, a cambio, obtiene previsibilidad regulatoria y mercado unificado.
Cuando ese equilibrio se desajusta —por precios desproporcionados o evidencia insuficiente— se erosiona la legitimidad del sistema.
Un arbitraje entre ciencia y conciencia
Las decisiones regulatorias de 2026 evidencian que la medicina contemporánea es un ejercicio constante de arbitraje entre innovación, equidad y sostenibilidad.
El éxito europeo no dependerá únicamente del número de moléculas autorizadas, sino de su capacidad para integrar simultáneamente eficiencia tecnológica, precisión terapéutica y estabilidad financiera de los sistemas públicos.
La cuestión estratégica ya no es si Europa puede innovar, sino si puede sostener esa innovación sin fracturar su modelo de solidaridad sanitaria. En esa tensión se definirá el próximo capítulo de la medicina europea.
La legitimidad futura de la medicina europea dependerá no solo de su capacidad de avanzar, sino de su capacidad de decidir con prudencia qué avances merecen ser financiados colectivamente.
Fuentes recomendadas
Comunicados oficiales del CHMP – EMA
European Public Assessment Reports (EPAR)
ECDC (datos epidemiológicos y vacunación)
OECD – Health at a Glance
IQVIA y EFPIA (datos de gasto farmacéutico)
`#InnovaciónRegulatoria2026` `#EmaBioTech` `#HoyLunes` `#EhabSoltan` #EMA #SaludPública #MedicinaDePrecisión
Este contenido es meramente informativo y no sustituye la consulta médica profesional.









